【产品名称】
英文名称:Luteinizing Hormone Test kit(Colloidal Gold Method)
【包装规格】
条型/卡型/笔型:单人份/袋;单人份/盒;2人份/盒;3人份/盒;4人份/盒;5人份/盒;6人份/盒;7人份/盒;8人份/盒;9人份/盒;10人份/盒;11人份/盒;12人份/盒;13人份/盒;14人份/盒;15人份/盒;16人份/盒;17人份/盒;18人份/盒;19人份/盒;20人份盒;25人份/盒;30人份/盒;40人份/盒;50人份/盒;60人份/盒;70人份/盒;80人份/盒;90人份/盒;100人份/盒;150人份/盒;200人份/盒;300人份/盒。
卡型+条型:各1人份/盒;各5人份/盒;各10人份/盒; 5人份/盒(2卡型+3条型);8人份/盒(3卡型+5条型);13人份/盒(3卡型+10条型);14人份/盒(4卡型+10条型);15人份/盒(5卡型+10条型)
笔型+条型:各1人份/盒;各5人份/盒;各10人份/盒;5人份/盒(2笔型+3条型);5人份/盒(3笔型+2条型);8人份/盒(3笔型+5条型);13人份/盒(3笔型+10条型);14人份/盒(4笔型+10条型);15人份/盒(5笔型+10条型)
【预期用途】
本产品可定性测定女性尿液中的促黄体生成素(LH)。
女性尿液中促黄体生成素浓度随着月经排卵周期变化而变化。LH高峰一经出现,预示24-36小时卵巢排卵,此时为最佳受孕时间。通过检测尿液中LH峰水平,明确排卵功能是否正常,预测排卵日期,能指导受孕和避孕的最佳时机,对不孕症、优生优育和安全期避孕的妇女起到良好的指导作用。临床应用单克隆与多克隆抗体相结合的酶联免疫测定法和磁性微粒分离免疫酶联法测定尿液和血液中LH浓度。
【检验原理】
促黄体生成素检测试剂盒(胶体金法)依据双抗体夹心法的原理,以硝酸纤维素膜为固相包被材料,以吸附力较强的聚酯膜作为金标记抗LH的吸附材料。检测时,被测样本中促黄体生成素(LH)与反应体系的金标记抗LH抗体结合,形成金标抗体复合物,继而此复合物继续迁移,再与硝酸纤维素膜上检测区包被的抗体相遇结合,形成双抗体夹心反应,显示有一紫红色沉积反应线,过量的金标抗体越过检测区与上部对照区抗体结合,形成第二条紫红色沉积反应线,若被检样本中没有LH,则无法形成双抗体夹心反应,只在对照区形成一条紫红色沉积反应线。依据检测区和对照区的紫红色线颜色判断检测结果。
【主要组成成分】
试纸条由硝酸纤维素膜(对照线C含羊抗鼠抗体、检测线T含单克隆抗LH抗体)、胶体金垫(含聚酯膜、氯金酸、单克隆抗LH抗体)、样品垫(含玻璃纤维)、基板和粗纤维吸水纸组成。
条型试剂盒由1支试纸条、1支干燥剂组成。
卡型试剂盒由1支试纸条、塑料外壳、1支干燥剂,1支吸管组成。
笔型试剂盒由1支试纸条、塑料外壳、1支干燥剂组成。
【储存条件及有效期】
本产品应储存于4-30℃、避光、干燥处,有效期为36个月。
产品打开包装后,应1小时内使用。
生产日期及失效日期见产品外包装。
【样本要求】
1.本试剂盒适用于尿液。
2.样本收集:尿样必须收集于干燥、清洁的容器内。
3.最佳采集尿液时间为上午10点至下午8点,尽量采用每天同一时间的尿样。不要使用第一次晨尿进行检测,因其不能正确反映尿液中LH真实水平。
4.采尿样前2小时内禁饮水,以免尿液被稀释。
5.收集的尿液样本如不能及时检测,可于2~8℃条件下保存72小时,检测前需平衡至室温。
【检验方法】
1.首先,确定被检者月经周期,即上次月经第一天到下次月经前第一天为一个周期。再按下表开始第一天的检测。每日一检,连续检测五天或至开始出现LH峰水平。如果月经周期少于21天或长于38天,被检者应遵医嘱进行检测。如不能确定月经周期,可按照平均28天来算,在月经完后的第11天开始测试。每天检一次,持续5天,或直到测出LH峰。
月经周期 检测开始日 月经周期 检测开始日
21天 第4天 30天 第13天
22天 第5天 31天 第14天
23天 第6天 32天 第15天
24天 第7天 33天 第16天
25天 第8天 34天 第17天
26天 第9天 35天 第18天
27天 第10天 36天 第19天
28天 第11天 37天 第20天
29天 第12天 38天 第21天
2.沿铝箔袋切口部位撕开,取出试剂盒进行检测。
3.检测方式
3.1条型检测:将试剂盒插入样品中(试剂盒插入样品深度不可超过标志线),当液体移行至测试区时,将其取出,放置在另一平面台上。
3.2卡型检测:用吸管吸取待检尿样0.2 mL(约3-4滴)于加样区中。
3.3笔型检测:将笔帽取下,在小便时让尿液直接淋在加样区,并且维持3秒钟的接尿时间(注意:尿液不要超过箭头,以免尿液弄湿测试区,影响检测结果)。
4. 5-10分钟观察测试区的显示结果,30分钟后的
显色结果无临床意义。
【阳性判断值】
本产品为定性结果,当人体尿液样本中促黄体生成素(LH)浓度不低于25 mIU/mL时,检测结果为阳性。
依据12个批次600个样本临界值检测结果,当样本中促黄体生成素(LH)浓度不低于25 mIU/mL时,各批号各型式的产品均能检出阳性,由此判定,临界值为25 mIU/mL。
【检验结果的解释】
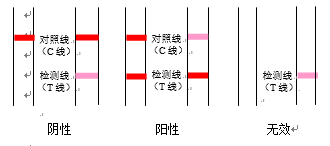
阴性:测试区中出现一条紫红色线(对照线C线)或出现两条紫红色线(对照线C线和检测线T线),但T线显色弱于C线,表明尿液LH水平低于25 mIU/mL,未出现LH峰水平。
阳性:测试区中出现两条紫红色线(对照线C线和检测线T线),且T线显色等于或强于C线,表明尿液中的LH水平等于或高于25 mIU/mL。表明未来24-48小时内即将排卵。
无效:测试区无紫红色线出现或仅出现一条紫红色线(检测线T线),表示检测失败或试剂盒无效,应重新测试。
图示如下:
【检验方法的局限性】
本产品适用于排卵检测,仅用于一次性体外诊断的定性检测,不能作为诊断的唯一标准。
【产品性能指标】
1物理性状
1.1 外观:试剂盒应整洁完整,无毛刺、无破损、无污染;材料附着牢固。
1.2 膜条宽度:膜条宽度应≥2.5 mm。
1.3 液体移行速度:液体移行速度应不低于10 mm/min。
2.临界值:当人体尿液样本中促黄体生成素(LH)浓度不低于25 mIU/mL时,检测结果为阳性。
3.特异性:本产品与浓度为200 mIU/mL的促卵泡激素(FSH)和250 µIU/mL的促甲状腺素(TSH)不发生交叉反应。
4.重复性:使用同一批号本产品平行检测25 mIU/mL LH 10次,反应结果一致,显色度均一。
5 稳定性:检测试剂盒有效期为三十六个月,取到有效期后一个月内的样品进行检测,应能达到1-4的要求。
6 批间差:取三个批号的LH试剂盒,检测浓度为25 mIU/mL的LH样品液,反应结果应一致,显色应均一。
【注意事项】
1.本产品仅用于一次性体外诊断用。
2.请在有效期内使用,当确定使用时再将包装打开。
3.与所有的诊断试验类似,诊断结果须综合所有临床信息和实验室结果后,由医生做出最后结论。
4.测试结果不受镇疼药、抗生素及其他普通药物的影响。服用含有HCG和LH成分的药物后,该检测会受影响,因此测试期间禁服此类药物。
5.孕期或绝经期妇女不适合该检测。
【参考文献】
1.许叔祥;标记免疫方法及仪器进展[J];上海医学检验杂志,1999,(05).
2.刘风娟;5种预测排卵方法准确性的临床观察[J];中国计划生育学杂志2010(06):354-356.
3.蒋海瑛,李唯亚,许佩兰,邵安安,杨华;两种尿LH排卵预测试纸的临床评估[J];浙江使用医学;2004,04.
【基本信息】
注册人/生产企业名称:青岛爱博检测科技有限公司
住所:山东省青岛市即墨市金口镇万亩方四路2号
联系方式:邮编266213 电话0532-89068567
售后服务单位名称:青岛爱博检测科技有限公司
联系方式:邮编266213 电话0532-87681668
生产地址:山东省青岛市即墨市金口镇万亩方四路
2号
生产许可证编号:鲁食药监械生产许20170001号
【医疗器械注册证书编号/产品技术要求编号】鲁械注准20162400575
【说明书核准及修改日期】2022年06月10日









